Carbonato de Cálcio PA ?Reagente puro para análise Altere os dados abaixo caso não seja igual o que consta no rótulo do seu reagente.
CaCO3
Propriedades: Cristais incolores ou pó branco, granulado ou cristalino; A forma anidra é higroscópica, a forma decaidratada eflorescente.
Massa molecular: 105,99 g/mol
Equivalente-grama: 52,995 g
Densidade: 1,84 g/cm3 (96-98% pureza de ácido)
Solubilidade: em água à 20° C é 220g/L - Pouco solúvel em etanol ; insolúvel em acetona.
O Carbonato de Cálcio é o sal dissódico do ácido carbônico com propriedade alcalinizante. Quando dissolvido em água , o Carbonato de Cálcio forma ácido carbônico e hidróxido de sódio . Como base forte, o hidróxido de sódio neutraliza o ácido gástrico, agindo assim como um antiácido.
A solução de Carbonato de Cálcio 0,1N obtida de Na2CO3 puro é considerada uma solução padrão primária, sem necessitar que seja padronizada. É superior à solução de NaOH como solução padrão alcalina.
Sinônimos: • Carbonato de Cálcio • Cinza de refrigerante • Carbonato dissódico • Sal dissódico de ácido carbônico • Carbonato de Cálcio • Refrigerante calcinado • Refrigerante Solvay • Ácido carbônico, sal dissódico • Carbonato de Cálcio • Soda calcinada • Cinza clara • Carbonato bissódico • Cinza de Soda Leve • Carbonato de cristal • Refrigerante anidro • Cinza de sódio leve • Carbonato de Cálcio seco • Soda anidra, 99,999%, pó • Carbonato de Cálcio, anidro, granular, grau de metais residuais, 99,99% • Carbonato de Cálcio, (99% como Carbonato de Cálcio ou 58% como óxido de sódio), grau técnico, leve
Disposição de resíduos
O Carbonato de Cálcio deve ser dissolvido em grande excesso de água e cuidadosamente neutralizado. tomando-se precaução para evitar aquecimento e evolução de vapores. os sólidos insolúveis que se formem devem ser separados e enviados a aterro “classe 1”.
Referências
MORITA, T.; ASSUMPÇÃO, R. M. V. Manual de Soluções Reagentes e Solventes. 2ª ed. Editora Edgard Blucher, 2007.
SODIUM CARBONATE - PUBCHEM. Disponível em: <https://pubchem.ncbi.nlm.nih.gov/compound/10340>. Acesso em 12 out 2023.
Diluição do Carbonato de Cálcio 3M (mol/L) para 1 M (mol/L) - 1000 mL

1 Separe o Carbonato de Cálcio 3 M (mol/L) em um béquer;

2 Retire 333,33 mL com auxílio de uma pipeta ou proveta;
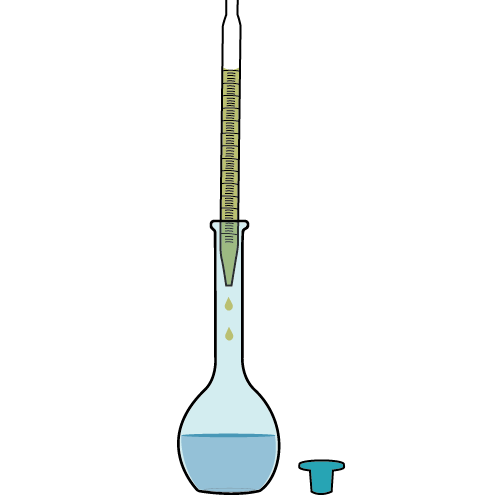
3 Transfira para um balão volumétrico de 1000 mL;
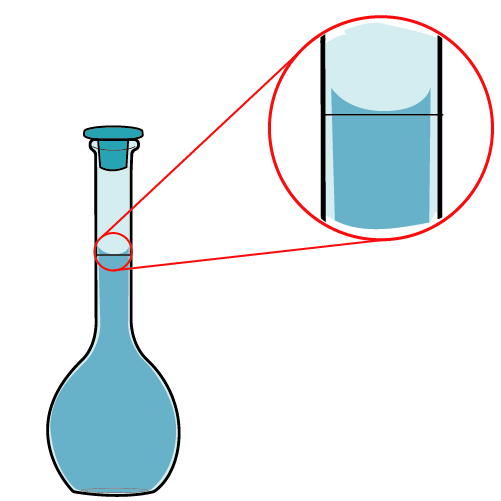
4 Avolume com água destilada até o traço de referência e homogenize.
Pó ou grumos brancos contendo 99% ou mais de pureza.
Água destilada
Água obtida após processo de destilação.
-
Solução de Carbonato de Cálcio
↪0,20N10,60g/L1,06%m/v↪1,00L* Se dissolvido somente em água é quase insolúvel, logo usa-se a parte superficial da solução.
1 Pese 10 g de Carbonato de Cálcio PA (100%);

2 Dissolva com pequena quantidade de ácido clorídrico diluido;

3 Transfira para um balão volumétrico de 1000 mL;

4 Avolume com água destilada até o traço de referência e homogenize.
-
Outras concentrações
Solução de Carbonato de Cálcio (Uso em padronização de água de sabão) - 1L
Dissolva 2 g de Carbonato de Cálcio PA (100%) com pequena quantidade de ácido clorídrico diluído e completa-se com água destilada até 1 Litro em um balão volumétrico, homogenize. Guarde em um frasco e rotule.
-
Continua depois da publicidade
Solução de Carbonato de Cálcio 20 g/L - 1L
Dissolva 20 g de Carbonato de Cálcio PA (100%) com água destilada até 1 Litro em um balão volumétrico, homogenize. Guarde em um frasco e rotule.
-
-
Referências
MORITA, T.; ASSUMPÇÃO, R. M. V. Manual de Soluções Reagentes e Solventes. 2ª ed. Editora Edgard Blucher, 2007.
